Rapport etter tilsyn ved Vestre Viken HF – håndtering av blod, blodkomponenter, celler og vev 2020
Oppfølging av tilsynet
I dette tilsynet ble det ikke avdekket lovbrudd. Tilsynet er derfor avsluttet.
Statens helsetilsyn har i perioden 7. januar – 4. august 2020 gjennomført tilsyn ved Vestre Viken HF. Tilsynet omfattet håndtering av blod, blodkomponenter, celler og vev og ble utført i henhold til følgende forskrifter:
- Forskrift om tapping, testing, prosessering, oppbevaring, distribusjon og utlevering av humant blod og blodkomponenter og behandling av helseopplysninger i blodgiverregistre (blodforskriften)
- Forskrift om krav til kvalitet og sikkerhet ved håndtering av humane celler og vev
Formålet med tilsynet var å undersøke om ledelsen ved Vestre Viken HF sikrer et høyt beskyttelsesnivå for mottakere og givere/donorer, hindrer overføring av sykdom og trygger sikkerheten og kvaliteten på blod, blodkomponenter, celler og vev.
Tilsynet ble gjennomført som en kombinasjon av informasjons- og dokumentinnhenting og videomøter med intervju av involvert personell og deres ledere. Videomøtene fant sted i perioden 15.-18. juni 2020.
Det ble ikke avdekket avvik innen de reviderte områdene. Tilsynet betraktes derfor som avsluttet.
1. Tilsynets tema og innhold
Statens helsetilsyn fører jevnlige tilsyn med håndtering av blod, blodkomponenter, celler og vev. Tilsynet gjennomføres etter lov om statlig tilsyn med helse- og omsorgstjenesten m.m. § 1, blodforskriften § 5-1 annet ledd og forskrift om krav til kvalitet og sikkerhet ved håndtering av humane celler og vev § 56.
Hensikten med tilsynet var å undersøke om ledelsen ved Vestre Viken HF sikrer et høyt beskyttelsesnivå for mottakere og givere/donorer, hindrer overføring av sykdom og trygger sikkerheten og kvaliteten på blod, blodkomponenter, celler og vev.
Vi har i dette tilsynet lagt spesielt vekt på følgende:
- Håndtering av blod og blodkomponenter for transfusjon:
- hindring av sykdomsoverføring via blod og blodkomponenter, herunder utvelgelse av blodgivere
- bestilling, valg, utlevering og transport av blod og blodkomponenter
- sporbarhet - mulighet til å identifisere blod og blodkomponenter fra giver til mottaker og omvendt
- samarbeid mellom Vestre Viken HF og eksterne virksomheter ved transfusjon
- Håndtering av humane celler og vev, inkludert testing av donorer av celler og vev:
- samsvar mellom helseforetakets praksis og godkjenning(er) etter forskrift om håndtering av humane celler og vev
- smittetesting av donorer av celler og vev
2. Aktuelt lovgrunnlag for tilsynet
2.1 Lovgrunnlag
Helsetilsynet er gitt myndighet til å kontrollere om virksomheter som håndterer blod, blodkomponenter celler og vev etterlever gjeldende lov- og forskriftsbestemmelser.
Lovgrunnlag for tilsynet:
- lov om spesialisthelsetjenesten m.m. (spesialisthelsetjenesteloven)
- lov om statlig tilsyn med helse- og omsorgstjenesten m.m. (helsetilsynsloven)
- lov om kommunale helse- og omsorgstjenester m.m. (helse- og omsorgstjenesteloven)
- lov om helsepersonell m.v. (helsepersonelloven)
- forskrift om tapping, testing, prosessering, oppbevaring, distribusjon og utlevering av humant blod og blodkomponenter og behandling av helseopplysninger i blodgiverregistre (blodforskriften)
- forskrift om krav til kvalitet og sikkerhet ved håndtering av humane celler og vev (forskrift om håndtering av humane celler og vev)
- forskrift om ledelse og kvalitetsforbedring i helse- og omsorgstjenesten (forskrift om ledelse og kvalitetsforbedring i helsetjenesten)
Blodforskriften og forskrift om håndtering av humane celler og vev har egne bestemmelser om internkontroll. Disse kommer i tillegg til, og utfyller de generelle bestemmelsene i forskrift om ledelse og kvalitetsforbedring i helsetjenesten.
Transfusjon av blod og blodkomponenter krever samhandling mellom involvert personell ved blodbanker og/eller transfusjonsenheter og kliniske avdelinger. Kravene til sporbarhet og dokumentasjon av gjennomførte transfusjoner i pasientjournal er utdypet i blodforskriften. Oppgaver knyttet til selve transfusjonen er regulert i den generelle helselovgivningen.
De aktuelle forskriftene er hjemlet i flere ulike lover. Der det er relevant har vi valgt å hjemle avvik direkte i aktuell forskrift.
2.2 Nærmere om forsvarlighet
Det er et grunnleggende krav til helsetjenesten at den helsehjelpen som ytes er faglig forsvarlig.
Kravet om forsvarlighet er en rettslig standard. Dette innebærer at innholdet bestemmes med utgangspunkt i normer utenfor loven. Disse normene er forankret i anerkjent fagkunnskap, faglige retningslinjer og samfunnsetiske normer, og utgjør det som betegnes som god praksis. Samtidig danner normene utgangspunkt for å fastlegge hvor grensen mot det uforsvarlige går.
Kravet om forsvarlighet er også et krav om forsvarlig organisering av tjenesten. I dette ligger blant annet at det gjennomføres organisatoriske og systemmessige tiltak som gjør det mulig for helsepersonellet å oppfylle plikten til forsvarlig yrkesutøvelse. Det følger av dette at virksomheten må styre sin drift med siktemål om at tjenestene er i samsvar med god praksis.
Det er en nær sammenheng mellom kravet til forsvarlighet, kravet til internkontroll og systematisk arbeid for å ivareta pasientenes sikkerhet, jf. helsetilsynsloven § 3 og forskrift om ledelse og kvalitetsforbedring i helse- og omsorgstjenesten.
2.3 Nærmere om forsvarlighet ved utlevering av blod til transfusjon i kommunehelsetjenesten – norm
Blodmottakere skal være sikret forsvarlige transfusjonstjenester uavhengig av hvor de mottar behandling. Ledelsen ved virksomheter som samarbeider om å utføre transfusjoner, eksempelvis helseforetak og kommuner, skal sørge for implementerte retningslinjer og tydelig ansvars- og oppgavefordeling for alle involverte.
Når blod og blodkomponenter transfunderes utenfor spesialisthelsetjenesten skal statlige helseinstitusjoner, eller institusjoner som mottar tilskudd fra regionale helseforetak til sin virksomhet, sørge for at ansatte i spesialisthelsetjenesten settes i stand til å oppfylle plikten til å gi råd, veiledning og opplysninger om helsemessige forhold. Hensikten er at den kommunale helse- og omsorgstjenesten settes i stand til å løse sine lovpålagte oppgaver.
Etter spesialisthelsetjenesteloven § 6-3 skal helseforetaket tilby veiledning til involvert personell og etablere retningslinjer for melding av uønskede hendelser, pretransfusjonsundersøkelser, bestilling, klargjøring, pakking og transport av blod og blodkomponenter. I tillegg skal det foreligge rutiner for å sikre sporbarhet, dokumentasjon og tilbakerapportering av utførte transfusjoner.
Retningslinjer, samarbeid og informasjonsutveksling knyttet til utlevering av blod og blodkomponenter beregnet for transfusjon i kommunehelsetjenesten er ment å utgjøre sikkerhetsbarrierer for å hindre feiltransfusjoner med påfølgende pasientskade eller død.
2.2 Avvik og merknad
Avvik er mangel på oppfyllelse av krav gitt i eller i medhold av lov eller forskrift.
Klassifisering av avvik:
- Kritisk avvik (K): Avvik som utgjør en signifikant risiko for skade på donor eller mottaker av blod, celler, vev og/eller organer.
- Stort avvik (S): Ikke kritisk avvik som utgjør en indirekte risiko for sikkerheten til donor og mottaker av blod, celler, vev og og/eller organer ved:
- avvik fra gjeldende myndighetskrav for håndtering av blod, celler, vev og/eller organer
- svikt i prosedyrene for frigivelse av blod, celler, vev og/eller organer til bruk på mennesker, eller at ansvarlig person ikke har utført sine legale plikter
- manglende godkjenning fra Helsedirektoratet for aktuell aktivitet
En kombinasjon av flere mindre mangler som hver for seg ikke utgjør et stort avvik, men som til sammen utgjør et stort avvik, skal rapporteres som det.
- Andre avvik (A): Avvik som ikke kan klassifiseres som kritisk eller stort, men som innebærer manglende samsvar med kravene til god praksis som følger av forskriftene for håndtering av blod, celler, vev og/eller organer.
Merknad er forhold som ikke er i strid med krav fastsatt i eller i medhold av lov eller forskrift, men der tilsynsmyndigheten finner grunn til å påpeke mulighet for forbedring.
Rapporten omhandler forhold som er avdekket under tilsynet og gir derfor ingen fullstendig tilstandsvurdering av virksomhetens arbeid innenfor de områder tilsynet omfattet.
3. Gjennomføring og deltakere ved tilsynet
3.1 Gjennomføring
Tidsrom for tilsynet, fra varsel ble sendt til ferdig rapport, var 7. januar – 4. august 2020.
Tilsynet ble gjennomført på følgende måte:
- Innhenting av informasjon i forkant av tilsynet.
Helsetilsynet sendte forespørsel til helseforetaket om antall utleverte enheter blod og blodkomponenter til transfusjon ved eksterne virksomheter i november 2018. Informasjonen ble mottatt 11. januar 2019.
- Varsel om tilsyn ble sendt 7. januar 2020.
Varselbrevet inkluderte et egenrapportskjema for aktiviteter som omfattes av de to forskriftene. Vestre Viken HF ble bedt om å fylle ut og returnere skjemaet til Helsetilsynet sammen med etterspurte dokumenter.
I varselbrevet informerte Helsetilsynet om at det ville bli gjennomført tilsynsbesøk ved en eller flere av blodbankene i helseforetaket. Hvilke blodbanker dette gjaldt ville bli besluttet etter mottak og vurdering av utfylt egenrapportskjema med vedlegg.
I varselbrevet ble det også informert om at tilsyn med smittettesting av donorer av celler og vev i utgangspunktet ville bli gjennomført ved informasjons- og dokumentinnhenting. Etter mottak og gjennomgang av egenrapportskjema med vedlegg ville vi vurdere om tilsynet også skulle inkludere tilsynsbesøk ved avdeling for laboratoriemedisin.
- Gjennomgang og vurdering av dokumenter
Oversikt over dokumenter Helsetilsynet har gjennomgått i forbindelse med tilsynet er gitt i vedlegg 1.
Etter gjennomgang av egenrapportskjema med vedlegg besluttet Helsetilsynet at det skulle gjennomføres tilsynsbesøk ved blodbankene i Drammen, Bærum og Kongsberg. Tilsyn med smittetesting av donorer av celler og vev ble besluttet gjennomført ved informasjons- og dokumentinnhenting.
- Endring i gjennomføring av tilsynet
Tilsynsbesøk var opprinnelig planlagt gjennomført i perioden 9.-13. mars 2020. På grunn av utbrudd av covid-19 i Norge, ble gjennomføringen endret:- Informasjon om at tilsynet var utsatt på ubestemt tid ble sendt helseforetaket 2. mars 2020.
- Etter dialog med helseforetaket ble brev om at tilsynet skulle gjenopptas sendt helseforetaket på e-post 22. mai 2020. For å ivareta krav om smittevern ble det besluttet at tilsyn med håndtering av blod og blodkomponenter skulle gjennomføres ved ytterligere dokumentinnhenting og videomøter med blodbankene i Drammen, Bærum, Kongsberg og Ringerike. Åpningsmøtet og sluttmøte ville bli gjennomført ved videomøter.
- Tilsynets videomøter ble gjennomført i perioden 15.–18. juni 2020. Program for videomøtene er gitt i vedlegg 2. Videomøtene omfattet
- åpningsmøte
- intervju med involvert personell og deres ledere
- sluttmøte med presentasjon av Helsetilsynets funn.
3.2 Deltakere
Deltakere fra Vestre Viken HF:
- Kontaktperson fra virksomheten: spesialrådgiver Bente Christin Monsen
- For oversikt over andre deltakere viser vi til vedlegg 3.
Deltakere fra Helsetilsynet:
- seniorrådgiver Elisabeth Try Valø (revisjonsleder)
- fagsjef Tone Blørstad (revisor)
- seniorrådgiver Tone Andersen (observatør)
4. Relevante forhold ved virksomheten
Vestre Viken HF har somatisk virksomhet ved Bærum sykehus, Drammen sykehus, Kongsberg sykehus, Ringerike sykehus og Hallingdal sjukestugu. Helseforetaket har også en psykiatrisk sykehusavdeling på Blakstad i Asker og fem distriktpsykiatriske sentre (DPS), tilbud innen barne- og ungdomspsykiatri samt tverrfaglig spesialisert rus- og avhengighetsbehandling. I tillegg har helseforetaket virksomhet ved 15 ambulansestasjoner.
Vestre Viken sitt opptaksområde omfatter 22 kommuner i Viken fylke, Innlandet fylke og Vestfold og Telemark fylke.
Helseforetaket har blodbankvirksomhet på sykehusene i Bærum, Drammen, Kongsberg og Ringerike samt tappestasjon på Hallingdal sjukestugu. Aktiviteten er tverrgående og organisert under avdeling for laboratoriemedisin, Medisinsk diagnostikk. Transfusjon av blod foregår ved de kliniske avdelingene i helseforetaket. I tillegg utleverer blodbanken, seksjon Bærum blod og blodkomponenter for transfusjon til ett privat sykehus.
Vestre Viken har godkjenning for testing av donorer av celler og vev ved avdeling for laboratoriemedisin, seksjon Bærum og seksjon Drammen.
5. Resultater fra tilsynet
5.1 Oppsummering antall avvik og merknader etc.
Det ble ikke avdekket avvik innen de reviderte områdene. Helsetilsynet har i merknad påpekt at helseforetaket bør inngå avtaler med eksterne virksomheter ved utlevering av blod og blodkomponenter for transfusjon dersom denne aktiviteten øker.
5.2 Generelt inntrykk
Helsetilsynet har merket seg at Vestre Viken
- har godkjenning for aktuell aktivitet knyttet til håndtering av blod, blodkomponenter, celler og vev.
- har gjennomført risikoanalyse og besluttet tiltak i forbindelse med utbrudd av Covid-19 som gjelder for håndtering av blod, blodkomponenter, celler og vev. Tiltakene er implementert i praksis.
- har innført elektronisk ID-kontroll og dokumentasjon ved transfusjon:
- Blod og blodkomponenter blir bestilt elektronisk i DIPS.
- Når blod og blodkomponenter hentes på blodbanken blir pasientens identitet kontrollert elektronisk mot blodpose og følgedokumenter ved at relevante data scannes inn i et eget dataprogram.
- Ved transfusjon gjennomføres dobbeltkontroll av pasientens identitet mot blodpose ved én manuell kontroll og én elektronisk kontroll. Den elektroniske kontrollen gjennomføres med en mobiltelefon som inneholder applikasjonen «Bedside Control Mobil». Kontrollen utføres ved at pasientens armbånd og blodpose scannes med mobiltelefonen. I tillegg dokumenteres tidspunkt for oppstart og avslutning av transfusjonen, samt om transfusjonen forløp komplikasjonsfritt. Dokumentasjon av ansatt som gjennomfører kontrollen gjøres ved å scanne ansattkortet. «Bedside Control Mobil» kommuniserer med blodbankens datasystem.

- har oppdaterte prosedyrer i elektronisk kvalitetshåndbok, og fortsetter det pågående arbeidet med å erstatte utvalgte lokale blodbankprosedyrer med overordnede prosedyrer som skal gjelde for blodbankene ved alle fire seksjoner.
- gjennomfører dokumentert opplæring, og benytter e-læringskurs for enkelte områder.
- registrerer avvik i helseforetakets elektroniske avvikssystem. Vestre Viken opplyste at de arbeider for å forbedre egen avvikshåndtering, eksempelvis ved økt læring og forbedring på tvers i hele organisasjonen etter avvik og uønskede hendelser.
- har utarbeidet 5-årsplan for internrevisjon. Internrevisjoner var gjennomført for områdene som var omfattet av tilsynet.
5.3 Håndtering av blod og blodkomponenter
Merknad:
Vestre Viken HF leverer sporadisk ut blod og blodkomponenter for transfusjon ved eksterne virksomheter. Helseforetaket har utarbeidet retningslinjer for denne aktiviteten. Helsetilsynet legger til grunn at oppgave- og ansvarsfordeling mellom partene blir regulert gjennom skriftlig avtaler dersom denne aktiviteten øker.
Faktiske forhold og begrunnelse for merknaden:
Vestre Viken har siste to år sporadisk levert ut blod og blodkomponenter for transfusjon til ett privat sykehus. Helseforetaket har utarbeidet prosedyren «BLB-IH Salg/eksport/forsendelse av blodprodukter til andre blodbanker» for å sikre at «forsendelse av blodprodukter utenfor eget sykehus foregår ensartet i Vestre Viken». I tillegg har helseforetaket siste år utarbeidet prosedyren «VV-BLB Blodtransfusjon utenfor sykehus» som gjelder for «leger og sykepleiere som er ansvarlige for transfusjon av erytrocytter utenfor sykehus i Vestre Viken». Den kommunale helsetjenesten er beskrevet som målgruppe for prosedyren. Helseforetaket har ikke utlevert blod og blodkomponenter for transfusjon i kommunehelsetjenesten siste to år.
Ved utlevering av blod og blodkomponenter for transfusjon utenfor eget sykehus stilles det strenge krav til blant annet distribusjon, utlevering, oppbevaring og dokumentasjon etter transfusjon, jf. blodforskriften §§ 3-1, 3-2 og 3-12. For å sikre at alle kravene etterleves, er det nødvendig at begge parter oppfyller sin del av forpliktelsene. Helsetilsynet vurderer at dette best kan sikres gjennom en forpliktende avtale mellom de to partene der oppgaver og ansvar er regulert.
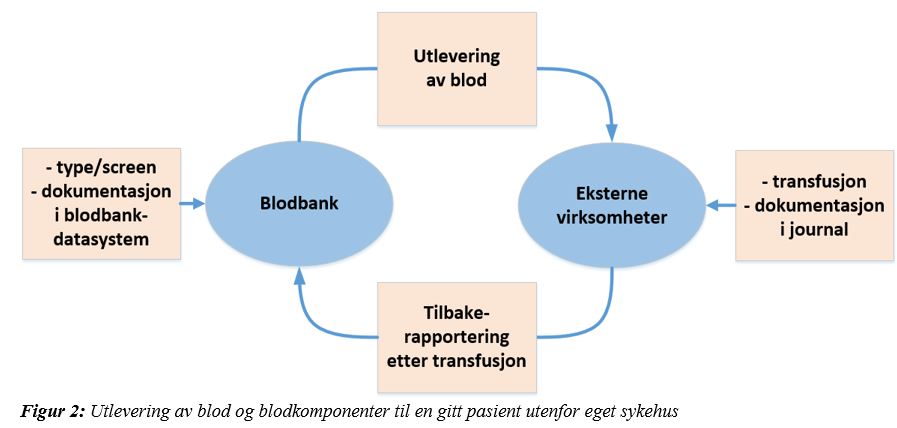
Ved utlevering av blod og blodkomponenter til kommunehelsetjenesten, har spesialisthelsetjenesten i tillegg en veiledningsplikt som beskrevet i kapittel 2.3.
5.4 Håndtering av humane celler og vev
Helsetilsynet gjennomførte dokumenttilsyn for området smittetesting av donorer av celler og vev. Bakgrunnen for denne beslutningen var følgende:
- Helsetilsyn gjennomførte tilsynsbesøk for området ved forrige tilsyn (2016). Ingen avvik ble avdekket.
- Medisinsk mikrobiologi, seksjon Drammen og seksjon Bærum er akkreditert.
- Aktuelle endringer var meldt til Helsedirektoratet.
- Internrevisjon var gjennomført siste to år. Foreliggende revisjonsplan for de neste to årene inkluderer smittetesting av donorer av celler og vev.
Innhentede dokumenter ga ikke grunnlag for å gjennomføre tilsynsbesøk i 2020.
Med hilsen
Mona Kaasa etter fullmakt
fung. avdelingsdirektør
Elisabeth Try Valø
seniorrådgiver
Brevet er godkjent elektronisk og sendes derfor uten underskrift
Vedlegg:1: Dokumentunderlag
2: Program for tilsynets videomøter
3: Deltakere under videomøtene
Kopi til:
Helsedirektoratet
Fylkesmannen i Oslo og Viken
Statens legemiddelverk
Bente C. Monsen, spesialrådgiver Vestre Viken HF
Saksbehandler: Elisabeth Try Valø, tlf. 21 52 99 83